|
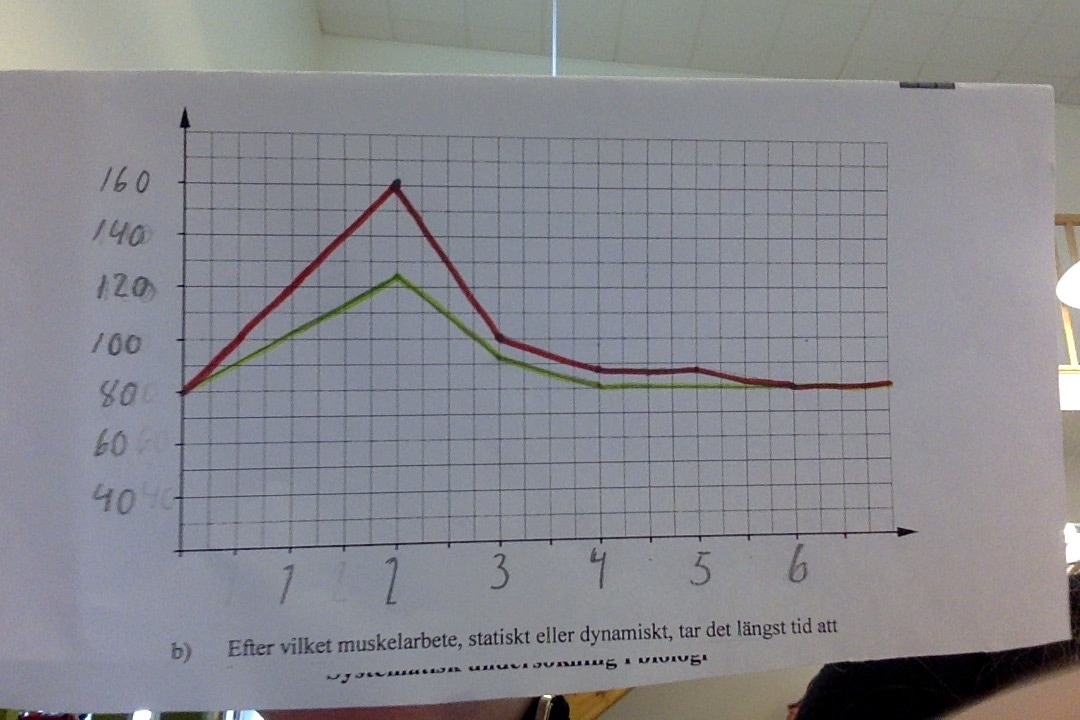
Syfte: Hur pulsen förändras under statiskt och dynamiskt muskelarbete, från vilopuls till arbetspuls och tillbaka till vilopuls. Hypotes: Jag tror att arbetspulsen kommer vara som högst vid dynamiskt muskelarbete samt att det kommer ta längst tid att återgå till vilopuls igen efter dynamiskt muskelarbete. Material: Tidtagarur Miniräknare Metod 1.Innan jag börjar med undersökningen lägger jag mig ner och slappnar av. 2.Efter att ha slappnat av ett tag mäter jag min vilopuls. 3.Jag räknar slagen i 15 sekunder och multiplicerar det med 4 så att jag får fram hur många slag i minuten. Jag mäter den två gånger för att vara säker. Sedan skriver jag ner resultatet 4.Efter det ska jag mäta hur pulsen jobbar vid statiskt muskelarbete, det ska jag göra genom att sitta i 90 grader mot en vägg. 5.Jag sitter i 90 grader i 2 minuter. 6.Direkt efter jag ställt mig upp mäter jag min arbetspuls på samma sätt som förra gången, räknar slag i 15 sekunder och multiplicerar resultatet med 4. 7.När jag räknat ut min arbetspuls skriver jag ner resultatet. 8.Jag mäter sedan pulsen en gång i minuten medan jag ligger ner och vilar tills jag nått vilopuls. 9.Sedan börjar jag med den dynamiska övningen, jumping jacks (x-hopp). 10. Jag gör övningen i 2 minuter och mäter sedan pulsen direkt när jag stannat. Jag skriver ner resultatet. 11. Precis som innan mäter jag pulsen, och antecknar, igen en gång i minuten tills jag nått vilopuls. 12.Till sist skriver jag ner resultatet. RESULTAT På tabellen kan man se att arbetspulsen blev högre när jag utförde den dynamiska övningen än när jag utförde den statiska övningen. Det tog även längst tid att återgå till vilopulsen efter det dynamiska arbetet än efter det statiska arbetet. 4 minuter efter det statiska arbetet hade pulsen gått tillbaka till vilopuls. Det tog hela 6 minuter för pulsen att återgå till vilopuls efter det dynamiska arbetet. Diagrammet visar samma sak som tabellen, min puls under statiskt samt dynamiskt muskelarbete.
Slutsats: Hela min hypotes stämde. Pulsen blev högre vid det dynamiska arbetet och det tog längre tid att återgå till vilopuls igen vid dynamiskt arbete än vid statiskt arbete. Arbetspulsen blev betydligt högre vid dynamiskt arbete än vid det statiska arbetet. Det beror på att många fler muskelgrupper aktiveras då än vid statisk träning. Vid det statiska arbetet jobbade ben-och sätesmusklerna medan alla muskelgrupper arbetade under det dynamiska arbetet. När musklerna arbetar ökar förbränningen i muskelcellerna. Musklerna behöver då mer syre och lämnar av mer koldioxid till blodet. Om musklerna inte hinner få nog mycket syre bildas mjölksyra. När koldioxidhalten i blodet ökar stimuleras andningsmusklerna vilket gör att andningen blir både djupare och snabbare. Blodet börjar då pumpas snabbare för att öka syretransporten till cellerna, då ökar även pulsen. Jag kände av att det skedde mer förbränning vid det dynamiska arbetet eftersom jag började få mjölksyra, musklerna behövde då mer syre än de hann få. Det tog längre tid att återgå till vilopuls igen efter det dynamiska arbetet. Det beror på att pulsen inte blev lika hög vid det statiska arbetet som den blev vid det dynamiska arbetet. Arbetspulsen vid statiskt arbete låg närmare vilopulsen än den gjorde vid dynamiskt arbete. När pulsen ligger närmare vilopuls tar det inte lika lång tid att återgå till den. Förbättringar: Bland de mer generella förbättringarna finns det flera saker jag skulle kunna göra bättre. Om jag hade gjort undersökningen flera gånger skulle resultatet blivit mer riktigt. Jag skulle kunna vara mer lugn så att pulsen inte går upp utan att jag ens gjorde något. Hade jag gjord övningarna en längre tid hade pulsen stigit ännu mer och resultaten skulle ha blivit säkrare. Jag kan vara ännu mer noggrann med tidtagandet. Om man råkar mäta pulsen fel med endast någon sekund blir resultatet felaktigt. Mer specifika förbättringar finns också att göra. Innan undersökningen började vilade jag för att få ner pulsen. Det gjorde jag genom att gå ut i korridoren och lägga mig ner på en bänk/soffa. I korridoren var det aningen livat och det gör att man inte får den riktiga vilopulsen. Om jag gjorde om undersökningen skulle jag hitta en lugnare plats där jag kan slappna av bättre. Direkt jag avslutade övningen skulle jag ha börjat ta pulsen. Det gjorde jag inte efter den statiska övningen, tappade bort mig och var därför tvungen att sitta 1 min extra för att kunna räkna pulsen direkt. Då satt jag alltså ca 3 min i 90°, fast gjorde endast jumping jacks i 2 min. När jag gjorde den statiska övningen använda jag ben- och sätesmusklerna. Med den dynamiska övningen använde jag alla muskelgrupper. Om jag hade gjort en dynamisk övning som tränade samma muskelgrupper, tex benböj, hade undersökningen blivit mer rättvis.
28 Comments
( OBS det gick inte att få in bilder) Förbränning av järnull Syfte: Jag ska undersöka vad som händer när järnull brinner. Hypotes: Jag tror att den sidan som brinner blir tyngre. När det brinner tror jag att elden ser ut som vanligt. När järnullen har brunnit klart tror jag att den blir svart. Material:
Metod:
Säkerhet: Man måste tänka på att inte ha något brännbart i närheten i fall att det skulle råka sprätta glöd. När man tar en järnullstuss måste man vara försiktig så att man inte skär upp händerna på de vassa trådarna. För att förebygga skärsår kan man använda tunna handskar eller helt enkelt vara väldigt försiktig. Eftersom att eld är inblandat i experimentet är det viktig att tänka på att hålla ett säkert avstånd från elden så att man inte bränner sig. Resultat: När man tände eld på järnullen såg man hur den började glöda och ändra färg. När den hade brunnit klart hade järnullstussen blivit mörkgrå. Inget av järnullen brann upp, utan den ändrade bara färg. Det var den sidan som brann som blev tyngst. Resultatet blev järnoxid, rost. Slutsats: Fe + O2+ värme = Fe2O3 4Fe + 3O2 + värme = 2Fe2O3 När man gör det här experimentet sker en kemisk reaktion. Järnet är i fast form och runtom järnullstussen kryllar det av syremolekyler som sitter ihop två och två. Värmen från elden tvingar syremolekylerna att dela på sig. Syremolekylerna fastnar sedan i järnatomerna. Eftersom att molekyler väger och det blir fler molekyler som sätter sig fast på järnullen blir det tyngre. Resultatet blir järnoxid i fast form. För att detta ska fungera måste det finnas minst 4 järnatomer och 3 järnmolekyler, annars finns det inte nog med byggstenar. Hypotes: Min hypotes stämde halvt, jag hade rätt om vilken sida som blir tyngst, men jag hade fel om hur slutresultatet såg ut. I min hypotes trodde jag att järnullen som brann skulle bli tyngre, det visade sig stämma. Jag trodde dock att elden skulle se ut som vanligt, men den såg mer ut som en glöd. När järnullstussen hade brunnit klart trodde jag att den skulle bli svart, men det visade sig att den bara blev en mörkare nyans av grå. Användningar i vardagen: Rost och kunskaper om rost går och är viktiga att använda i vardagen. För att järn ska rosta behövs vatten och syre. När man bygger hus och använder sig av järn, tex järn bjälkar, är det viktigt att man tänker på hur järnet rostar. Det finns flera olika sätt att stoppa järnet från att rosta, tex kan man sätta andra metaller över järnet. Många bilägare har ett stort problem med att bilen rostar. För att förebygga rost ska man regelbundet tvätta bilen. Bilarna målas och lackeras även för att skyddas så mycket som möjligt mot rost. Förbättringar för ett tydligare resultat: Lika stora järnullstussar. Om vi hade sett till att båda tussarna var lika stora hade det varit lättare att se ett exakt resultat. För att få lika stora tussar som väger exakt lika mycket kan man använda en vanlig våg. En stadigare våg. Den vågen vi använde till den här labben var ganska vinglig och ostabil vilket kan göra att resultatet inte blir helt riktigt. Om man använder en stadigare våg nästa gång kan resultatet bli ännu tydligare. Fortsatt undersökning: Genom att förbränna järnull fick vi fram järnoxid i fast form. Vad skulle hända om man sedan eldade järnoxiden? Skulle den fortfarande se likadan ut, skulle den byta form eller skulle den kanske brännas och bli helt svart? Frågeställningen skulle kunna vara: ”Vad händer när man eldar järnoxid”. Ändring av planering
För en ännu tydligare planering hade jag kunnat:
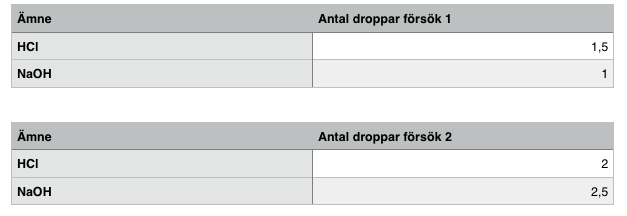
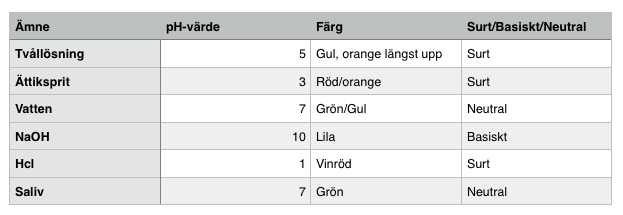
För att någon ska kunna följa en labbrapport är det viktigt att man skriver exakt hur man gör. Detta experiment kräver bara en liten bägare, till den räcker det med 40 ml vatten. Hade man tagit en större bägare hade man behövt mer vatten. Btb reagerar väldigt snabbt. Eftersom det finns miljarders joner i en liten droppe måste man vara väldigt försiktig när man droppar i ämnena så det inte blir för mycket. När jag gjorde detta experiment var en droppe alldeles för mycket, jag behövde endast en halv droppe, tom mindre. Om man inte rör om med glasstaven efter varje droppe man häller i får man inte fram helt rätt resultat. Den exakta färgen syns inte fören man har rört om och väntat en liten stund. Efter att man rört om och väntat ca 30 sek kan man hälla i nästa droppe. När man har bägaren direkt på det ljusbruna/beige bordet är det lite svårare att se exakt den färg vattnet i bägaren blir. Genom att ha ett vitt papper under lyfts färgen fram mer . Nu antecknade jag inte för varje droppe jag hällde i. Det gjorde att jag nästan glömde bort och var tvungen att tänka igenom noggrant exakt hur jag gjort. Om jag hade skrivit ner alla droppar jag hällde i skulle det ha underlättat mycket. Neutralisera vatten
Syfte: Neutralisera vatten med hjälp av NaOH och Hcl. Material:
Metod:
Säkerhet:
Felkällor:
Sammanfattning periodiska systemet
Grundämnenas periodiska system är en tabell som ryssen Mendelejev påbörjade på 1800-talet. Han kom på att om man ordnade alla grundämnen i en tabell efter hur många protoner som fanns i atomkärnan (atomnummer) så återkommer ämnena med liknande egenskaper regelbundet, det märker man när man skriver atomer med lika många elektroner i yttersta skalet under varandra. Man skriver också in atommassan för varje atomslag, den mäts i u (atommassenhet). Atommassan är ett medelvärde av alla olika isotoper av atomslaget som finns i naturen. Man har efterhand upptäckt nya grundämnen och kunnat fylla de luckor som uppstod i Mendelejevs tabell. Än så länge har man hittat 91 grundämnen, de flesta i naturen men vissa har också kunnat framställas i laboratorier. De grundämnen som finns i periodiska systemet delas in i grupperna metaller och ickemetaller. Det finns även vissa ämnen som man kallar för halvmetaller. Det periodiska systemet är indelat i grupper och perioder. De lodräta raderna i tabellen kallas grupper och de vågräta kallas för perioder. Det finns 7 perioder och 18 grupper. De ämnen som tillhör samma period har lika många elektronskal, hur många elektronskal atomerna har ser man på numret på perioden ämnet tillhör. Grundämnena som är indelade i samma grupp har liknande egenskaper, det beror på att de har lika många elektroner i de yttersta skalet, det kallas för valenselektroner. Ämnena i grupp 1 är väte och alkalimetallerna. De ämnena reagerar lätt med andra ämnen i naturen och kan därför inte hittas rena i naturen. Alkalimetallerna finns bara i kemiska föreningar och metallerna är så mjuka att de går att skäras med kniv. Ämnena i grupp ett har endast en valenselektron. Det gör att de väldigt gärna vill reagera med en atom med 7 valenselektroner. Grupp 17 innehåller Halogener. Dessa ämnen är ickemetaller som väldigt lätt reagerar med andra ämnen och förekommer därför inte i ren form i naturen, precis som ämnena i grupp 1. Ämnena i grupp 17 har 7 valenselektroner. Ämnena i grupp 1 och grupp 17 vill reagera med varandra för att få 8 valenselektroner, alltså ett fullt yttre skal. Grupp 18 innehåller ädelgaserna. Ädelgaserna reagerar mycket ogärna med andra ämnen. Det beror på att de har ett helt fullt yttre skal. Dessa ämnen bildar inte molekyler utan är bara ensamma atomer.
2. Hur skriver man den kemiska formeln för:
3. Vilka och hur många atomer ingår i följande molekyler:
Lätt att förstå:
Svårare att förstå:
12. Hur fångas nya kolatomer in i ett ekosystem? Kolatomer finns i luften som koldioxid. Växterna är de organismer i ekosystemet som kan ta upp koldioxiden genom fotosyntesen, djur har inte de organen för att kunna göra det. De använder sig sedan av koldioxiden till fotosyntesen, där de gör om den till fast form i bla socker. 13. Hur fångas nya kväveatomer in i ett ekosystem? Kvävgasen finns i luften och alla organismer är omringade av den. Men alla kan inte ta upp kvävgasen och göra om den till den form som är användbar för levnads organismer. Varken djur eller växter kan göra detta. Det är bara vissa bakterier som klarar av den uppgiften, cyanobakterier i vattnet och kvävefixerande bakterier i marken. Kväve kommer in i ekosystemet med vatten från marken. De sugs upp av växternas rötter och byggs då in i växterna. När växten dör bryter nedbrytare ner växten och kvävet åker ner i marken igen, eller så kommer ett djur kommer och äter de delarna som kvävet finns och kvävet förs det vidare in i djuret. När djuren sedan dör och blir nedbrutet av nedbrytare kommer kvävet ner i marken igen där det löser sig i vattnet. Då börjar allt om igen. Utmaningen 2: Kolmolekylerna börjar i luften i form av koldioxid. Sen kan ett träd eller en annan växt ”dra in” atomen för att använd den till fotosyntesen. Kolatomen kan vara fast i trädet flera flera år innan den kommer loss igen. Den kanske sitter fast i trädet tills det dör och nedbrytare kommer och frigör atomen igen, eller så kommer en älg och äter på trädet så att atomen hamnar i älgen. Det finns otroligt många saker som kan hända som gör att atomen blir ”fri” igen. Älgen kanske blir skjuten och uppäten, då hamnar atomen i den som åt upp älgen, eller så stannar den kvar i resterna av älgen till nedbrytare som kommer och bryter ner det sista. Det kan också vara så enkelt som att älgen bara andas ut atomen. |










 RSS-flöde
RSS-flöde
