|
A: Resultaten man kan få på en vanlig sexsidig tärning är 1,2,3,4,5,6. Anna tänker att det är lika stor sannolikhet att få en 1a som en 4a eller 6a. Joel tänker att det är svårast att få en 6a för att det är högst. Vi håller med Anna. När man slår en tärning som är helt omanipulerad är det lika stor sannolikhet att få vilket nummer som helst. Man fokuserar ofta på att få så högt nummer som möjligt och därför tänker man mer på gångerna man får låga nummer. B: De tänker att det är svårare att få 2 och 12 än något däremellan. Vi håller med Joel. Det är mindre sannolikhet att slå två av samma siffra än två av olika. Talen 2 och 12 går endast att få på ett sätt medan de flesta talen däremellan går att få på flera olika kombinationer. Störst sannolikhet är det att få talet 7 om man slår med två träningar. Det finns tre olika möjligheter att få 7, 6+1, 1+6, 5+2, 2+5, 4+3 och 3+4. 2 . 1 + 1
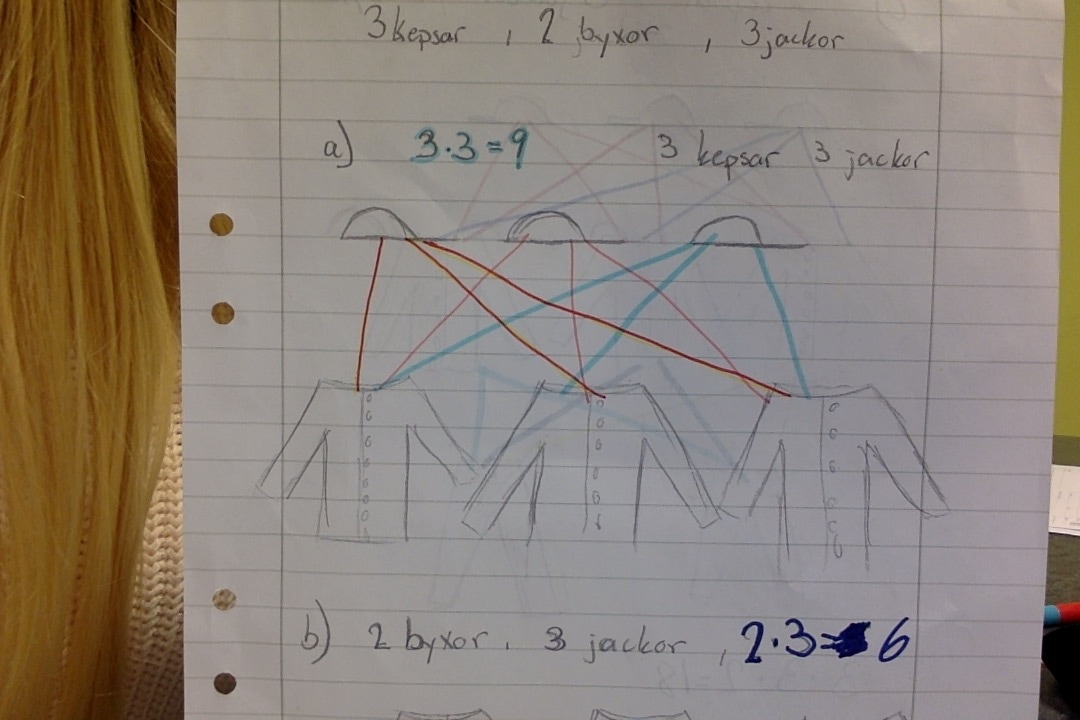
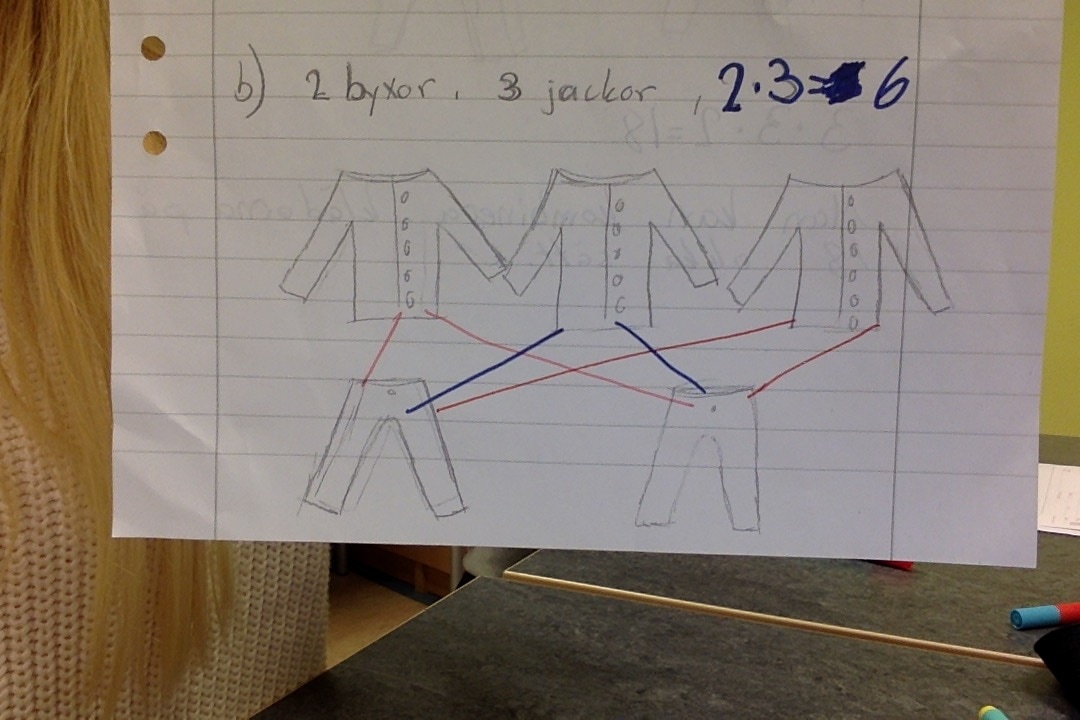
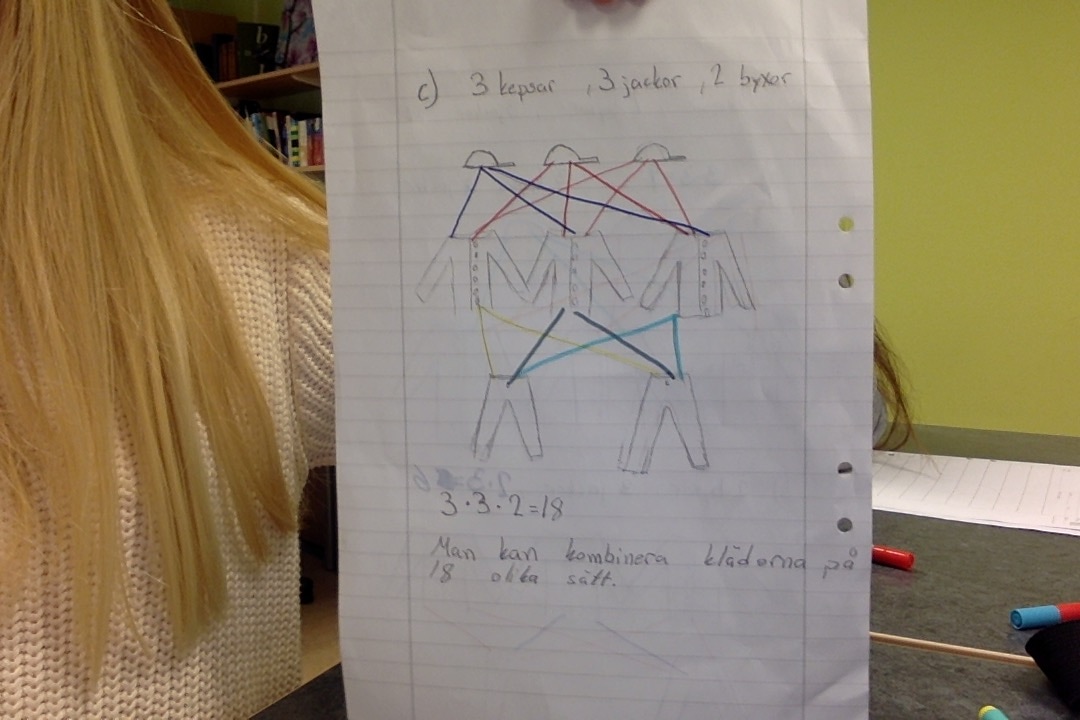
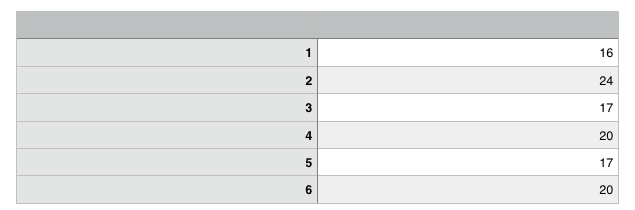
3 . 2 + 1 1 + 2 4. 2 + 2 3+ 1 1 + 3 5. 3 + 2 4 + 1 2 + 3 1 + 4 6 . 3 + 3 5 + 1 4 + 2 1 + 5 2 + 4 7. 3 + 4 5 + 2 6 + 1 4 + 3 2 + 5 1 + 6 8. 4 + 4 6 + 2 5 + 3 2 + 6 3 + 5 9. 4 + 5 6 + 3 5 + 4 3 + 6 10. 5 + 5 6 + 4 4 + 6 11. 5 + 6 5 + 6 12. 6 + 6 Här ser man att det är störst sannolikhet att få 7. Det finns 6 möjligheter att slå 7 med två tärningar. Minst sannolikhet är det att slå 12 eller 2. Det finns endast en möjlighet att slå 12 eller 2. (Det var svårt att få in tabellen och bilderna på bloggen så jag fick ta bild på rapporten istället)
Neutralisera vatten
Syfte: Neutralisera vatten med hjälp av NaOH och Hcl. Material:
Metod:
Säkerhet:
Felkällor:
Lab 1: Kalkvatten
1. Jämföra resultatet med frågeställningen och dra välutvecklade slutsatser med kopplingar till kemiska modeller och teorier. Vad händer när man blåser i kalkvattnet? Ca2+2OH+CO2(g) – 2 CaOH3 + H2O Innan man blåste CO2 i kalkvattnet var färgen nästan genomskinlig, men när man blåste i sugröret blev färgen grumlig, nästan vit. Det beror på att kalkvatten är en reagens på koldioxid. Kalkvattnet består av Ca(OH)2 + H2o. När det sker bildas lösa OH-joner och Ca2-joner. När man blåser genom sugröret tillförs CO2 till blandningen. Ämnena blandar om sig och ett nytt ämne bildas, CaCo3, kalciumkarbonat. Kalciumkarbonat är ett fast salt och vill inte blanda sig med vattnet. Därför blir vattnet grumligt. 2. Välutvecklade resonemang om resultatets rimlighet med tanke på felkällor. Resultatet är rimligt eftersom det blev detsamma för alla som labbade. Man vet säkert att kalkvatten är en reagens på koldioxid eftersom det gjorts tusentals experiment. 3. Ge förslag på hur undersökningarna kan förbättras. För att få ett ännu tydligare resultat borde jag ha diskat bägaren först så att det inte var något smuts kvar som kan ha gjort vattnet lite grumligt från början. Jag skulle kunna blåsa längre än vad jag gjorde nu. Om jag hade blåst 1 minut istället för ca 30 sekunder skulle vattnet kanske ha blivit grumligare och det hade varit större skillnad på vattnets färg från början och efter experimentet. Nu var det Susanne som blandade kalkvattnet, då kan vi inte veta helt säkert att det verkligen är kalkvatten eller om det är något annat. Nästa gång skulle vi kunna blanda kalkvattnet själv så att vi vet att det blir rätt. Kalkvattnet vi använde var inte nyblandat, det betyder att det redan finns lite koldioxid i vattnet som då blir lite grumligt. Om man har helt nyblandat kalkvatten skulle resultatet bli ännu tydligare. 4. Visa på nya tänkbara frågeställningar att undersöka. Vi vet redan att kalkvatten är en reagens på koldioxid. Men vad skulle hända om vi testade experimentet med en annan gas, syrgas exempelvis? Lab 2: Släcka eld med koldioxid 1. Jämföra resultatet med frågeställningen och dra välutvecklade slutsatser med kopplingar till kemiska modeller och teorier. Det första jag gjorde var att blanda bakpulver, några droppar ättika och vatten i en e-kolv, jag höll för e-kolven med handen. När bakpulvret kommer i kontakt med vattnet börjar den reagera med sig själv, det är syran som reagerar med bikarbonatet, det kan inte ske om det är torrt, ättikan är där för att rektionen ska gå fortare. När bakpulvret reagerar med sig själv bildas ett salt och koldioxid. Koldioxid är en tung gas, det gör så att den stannar kvar i flaskan även om jag skulle ha släppt handen, men att hålla för handen gör så att en ännu större mängd stannar kvar i flaskan. Den andra delen i experimentet var att hälla ner koldioxiden på ljuset. När bakpulvret reagerat med sig själv och koldioxid skapats släppte jag handen och hällde försiktigt ner gasen i ljuset. Som sagt är koldioxid en tung gas och går att hälla ner, hade det varit en lätt gas hade den flugit iväg åt alla håll. När koldioxiden rann ner på ljuset bildade gasen ett ”lock” över ljuset. Eftersom ljus behöver syre för att överleva och koldioxiden tog bort allt syre runt ljuset slocknade det. 2. Välutvecklade resonemang om resultatets rimlighet med tanke på felkällor. Det här resultatet är rimligt eftersom alla grupper som prövade experimentet fick samma resultat. Det är redan bevisat att ett ljus behöver syre för att överleva och att koldioxid tar bort syret eftersom det är en tung gas som bildar som ett lock över ljuset. Det här experimentet har gjorts många gånger och det har därför bevisats att resultatet är rimligt. Man använder koldioxidsläckare för att släcka eldsvådor. 3. Ge förslag på hur undersökningarna kan förbättras. För att vara ännu mer säker på att det är koldioxid som har bildats kan man hälla ner kalkvatten i e-kolven. Eftersom kalkvatten är en reagens på koldioxid kommer vattnet bli grumligt, då vet man säkert att det är koldioxid som bildats. När man häller över koldioxiden från e-kolven till ljuset är det viktigt att man inte råkar hälla ner saltet som bildats, om salt rinner ner i ljuset kan man inte veta om det var gasen eller saltet som släckte det. 4. Visa på nya tänkbara frågeställningar att undersöka. Man skulle kunna undersöka om det finns några andra gaser som kan släcka eld, men måste vara försiktig så man inte tar alldeles fel gas. Man skulle också kunna undersöka om det finns något annat ämnen än bakpulver som kan bilda koldioxid.
2. Hur skriver man den kemiska formeln för:
3. Vilka och hur många atomer ingår i följande molekyler:
Lätt att förstå:
Svårare att förstå:
|
Agnes EdelsvärdArkiv
September 2017
Kategorier |












 RSS-flöde
RSS-flöde
